到目前为止,在大多数的成人软组织肉瘤中并没有发现能够得到普遍认可的癌基因突变,这些肿瘤对目前临床上所使用的靶向治疗方法都不敏感。在最近发表在国际学术期刊Cancer Research上的一项研究中,来自美国宾夕法尼亚大学的研究人员对肉瘤发生机制进行了研究希望能够找到潜在的治疗干预方法。
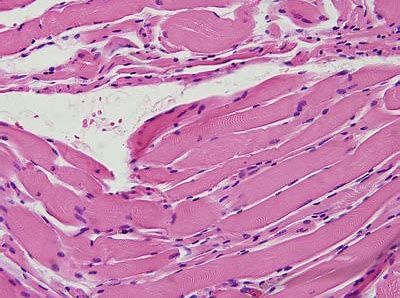
多形性未分化肉瘤(UPS)是一种具有侵袭性的肿瘤经常发现于骨骼肌中,并且会出现Hippo信号途径的失调及其转录效应因子YAP1的异常稳定,这些情况的出现都会促进细胞增殖和肿瘤发生。但是推动该信号途径失调的下游机制还没有得到完全了解。
在这项研究中,研究人员通过小鼠模型和全基因组分析,发现YAP1在一些肉瘤中发生持续激活,进一步的研究结果显示这种情况的出现是因为其抑制因子angiomotin(AMOT)发生了表观沉默。用组蛋白去乙酰化酶抑制剂vorinostat和JQ1进行处理能够重新恢复AMOT的表达,使Hippo信号途径恢复正常,进一步诱导肌肉分化程序并抑制肉瘤的发生。
研究人员还对YAP1促进肉瘤发生的下游机制进行更进一步的研究,他们发现YAP1能够通过抑制泛素特异性肽酶31(USP31)的表达促进肉瘤发生,而USP31是一个新发现的NF-kB信号途径的上游负调控因子。组蛋白去乙酰化酶抑制剂与其他肿瘤治疗药物联合使用能够有效恢复USP31的表达,导致NF-kB活性的下降。
综上所述,该研究发现了导致多形性未分化肉瘤发生的一个关键机制,也提示了通过靶向表观遗传修饰治疗肉瘤的可能性。
犬药代动力学
 苏公网安备 32058502010454号
苏公网安备 32058502010454号
